FEED ARTIGOS
| 2022 | ||
|
Desta vez o trabalho “Assessment of Pesticides in the Chasqueiro Irrigation District, Southern Brazil, an Agricultural Area of International Importance” de autoria de Marília Guidotti Corrêa, Sergiane Caldas Barbosa, Gabriel Borges dos Santos, Gilberto Loguercio Collares e Ednei Gilberto Primel será publicado no periódico Water, Air, & Soil Pollution (FI 2,984). Este trabalho é um dos resultados obtidos na tese de doutorado da aluna Marilia do Programa de Pós-graduação em Química Tecnológica e Ambiental (PPGQTA-FURG) sobre a ocorrência de agrotóxicos e a avaliação da qualidade da água da Lagoa Mirim e afluentes. Este trabalho contou com a parceria da Agência de Desenvolvimento da Bacia da Lagoa Mirim – UFPel. O trabalho contribuiu com a geração de dados, promovendo o conhecimento sobre a influência das atividades agrícolas em áreas adjacentes a Lagoa Mirim na qualidade de suas águas. Os resultados mostram a importância da criação de programas para controle e avaliação de agrotóxicos em distritos de irrigação, com o objetivo de proteger o meio ambiente. Para conferir mais, clica no link e boa leitura! https://link.springer.com/article/10.1007/s11270-022-05989-9
|
||
| 2022 | ||
|
|
||
|
O trabalho “Detoxification and effects of the UV filter Benzophenone-3 in the digestive gland and hemocytes of yellow clam (Amarilladesma mactroides) under a perspective of global warming scenario” de autoria de Fernanda Chaves Lopes, Micheli Rosa de Castro, Guilherme Toledo Alves Patrocinio, Amanda da Silveira Guerreiro, Sergiane Caldas Barbosa, Ednei Gilberto Primel e Camila de Martinez Gaspar Martins foi publicado no periódico Marine Pollution Bulletin (FI 7,001). Este trabalho é resultado de determinações cromatográficas de benzofenona-3 em amostras de marisco, fruto da parceria com o Profa. Camila Martins do Instituto de Ciências Biológicas da FURG. Para conferir mais, clica no link e boa leitura! https://doi.org/10.1016/j.marpolbul.2022.114188
|
||
| 2022 | ||
 |
||
|
Desta vez o trabalho “Polycyclic Aromatic Hydrocarbons (PAHs) in honey from stingless bees (Meliponinae) in southern Brazil” de autoria de Lucas Cavagnoli Marcolin, Jean Lucas de Oliveira Arias, Larine Kupski, Sergiane Caldas Barbosa e Ednei Gilberto Primel, será publicado na revista Food Chemistry (FI 9.231). Este trabalho é fruto do doutorado realizado pelo Lucas no Programa de Pós Graduação em Engenharia e Ciência de Alimentos, orientado pelo Prof. Ednei Gilberto Primel. Para conferir mais, clica no link e boa leitura! https://www.sciencedirect.com/science/article/abs/pii/S0308814622029065
|
||
| 2022 | ||
|
O artigo de revisão “Updated knowledge, partitioning and ecological risk of pharmaceuticals and personal care products in global aquatic environments” de autoria de Marisa de Jesus Silva Chaves, Jonatas Kulzer, Paula da Rosa Pujol de Lima, Sergiane Caldas Barbosa e Ednei Gilberto Primel está disponível no periódico Environmental Science: Processes & Impacts (FI: 5,3). Este trabalho de revisão teve início no período remoto, contando com a participação de estudantes e pesquisadores do grupo. Informações sobre os níveis de concentração de contaminantes emergentes em água, sedimento e organismos aquáticos em diferentes continentes foram tabeladas e discutidas de maneira a promover uma atualização dos níveis e locais de ocorrência destes contaminantes. O particionamento nos compartimentos ambientais também foi apresentado; assim como uma discussão sobre o perfil da ocorrência de contaminantes após o início da pandemia do COVID-19. Para conferir mais, clica no link e boa leitura! https://pubs.rsc.org/en/content/articlelanding/2022/em/d2em00132b
|
||
| 2022 | ||
|
Publicação nova saindo.. Desta vez o trabalho “Emerging Contaminants in Sediments as Markers of Anthropogenic Inputs in Santos Estuarine System: Analytical Method and Occurrence Data? de autoria de Marisa J. S. Chaves, Sergiane C. Barbosa, Ednei G. Primel e Ítalo B. Castro será publicado no periódico Journal of the Brazilian Chemical Society. Este trabalho é resultado da aplicação do método desenvolvido no mestrado da Marisa Chaves na investigação da ocorrência de contaminantes emergentes em amostras de sedimentos no sistema estuarino de Santos, fruto da parceria com o Prof. Ítalo Braga Castro (Instituto do Mar, Universidade Federal de São Paulo IMAR-UNIFESP). Este trabalho contribuiu com a geração de dados de concentrações ambientais, o que pode auxiliar na discussão da criação de listas prioritárias de contaminantes e guiar o estabelecimento de legislação sobre contaminantes emergentes no ambiente aquático. Para conferir mais, clica no link e boa leitura! http://static.sites.sbq.org.br/jbcs.sbq.org.br/pdf/2022-0124AR.pdf |
||
| 2022 | ||
|
Olá pessoal 👋 Mais um trabalho que acaba de ser publicado 👏 Desta vez o trabalho “Determination of Ochratoxin A and Its Metabolite Ochratoxin Alpha in Diferent Food Matrices After Enzymatic Biotransformation” de autoria de Larine Kupski, Duane Volpato, Caroline B. Rocha, Eliana B. Furlong, Sergiane C. Barbosa e Ednei G. Primel será publicado na Revista Food Analytical Methods. 📚 Este trabalho é fruto do pós doutorado realizado pela Prof. Larine Kupski, atualmente na Universidade Estadual de Maringá (UEM), supervisionado pelo Prof. Ednei Gilberto Primel. O trabalho foi desenvolvido no LACOM em colaboração com o Laboratório de Micotoxinas e Ciência de Alimentos (LAMCA). Para conferir mais, clica no link https://link.springer.com/article/10.1007/s12161-022-02349-5 e boa leitura!! |
||
| 2022 | ||
|
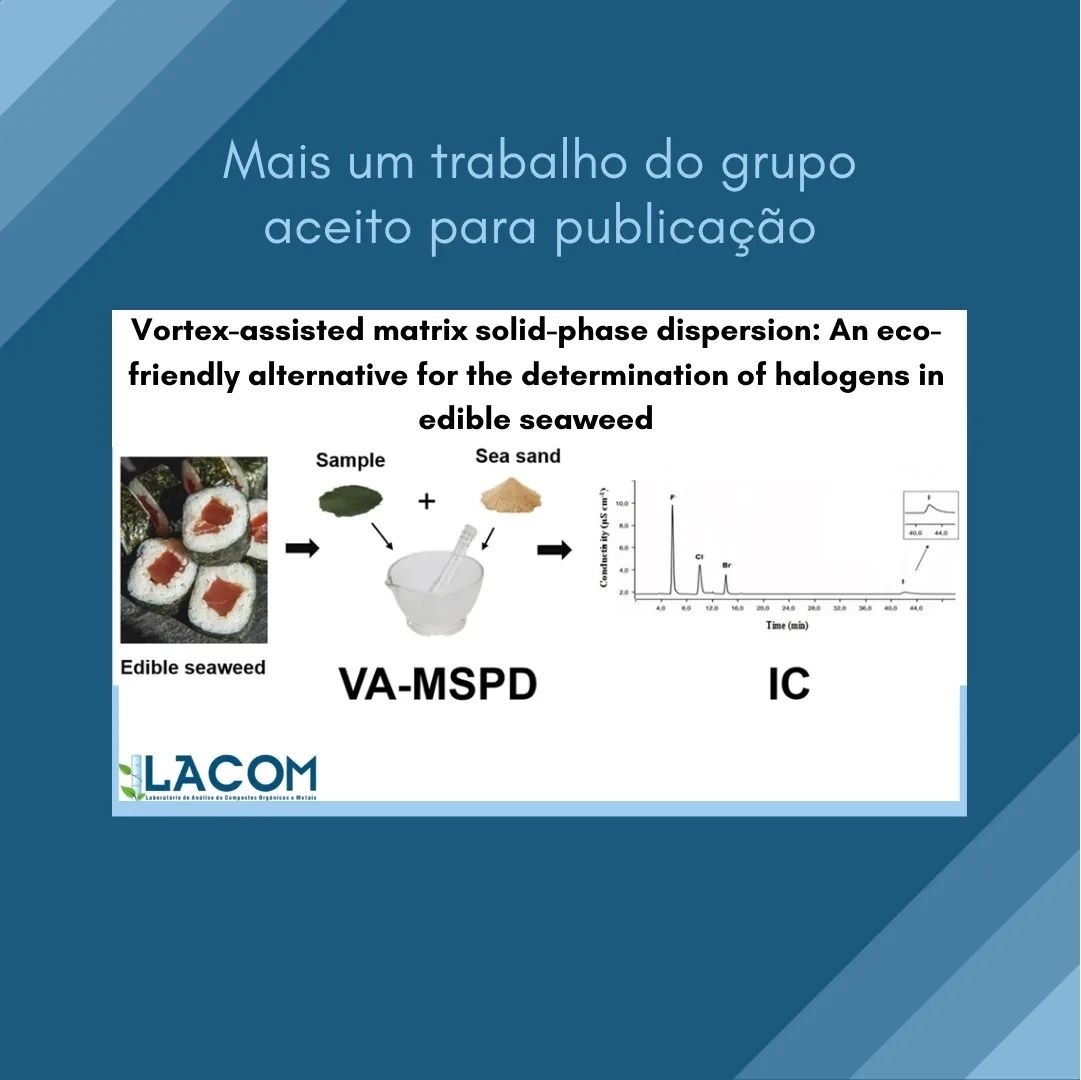
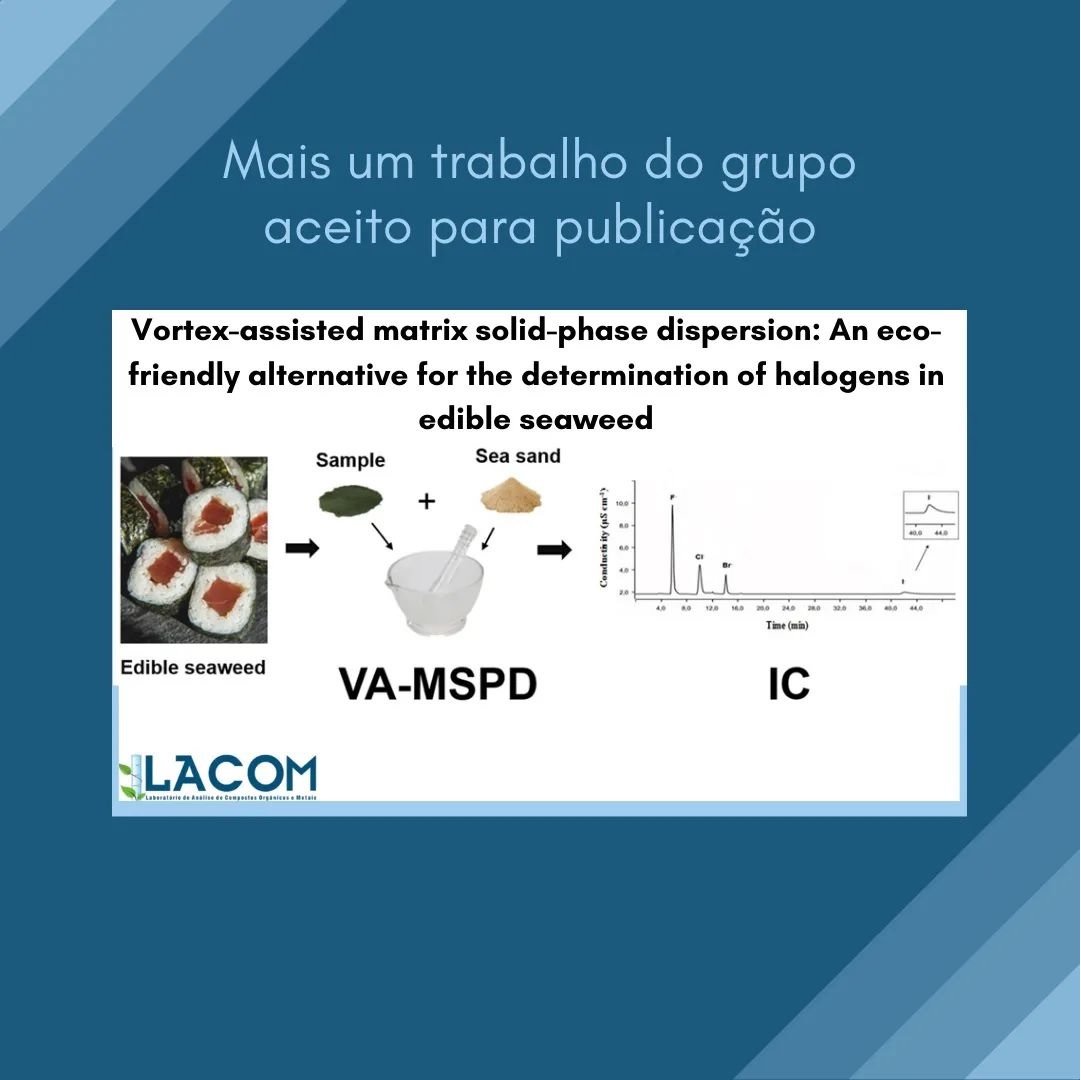
Olá pessoal 👋 Hoje viemos trazer mais um trabalho do grupo que acaba de ser aceito para publicação!!! 🤩 Desta vez o trabalho “Vortex-assisted matrix solid-phase dispersion: An eco-friendly alternative for the determination of halogens in edible seaweed” de autoria de Maiara Helena de Melo Malinowski, Paloma Konzgen Maciel, Marisa de Jesus Silva Chaves, Sergiane Caldas Barbosa, Ednei Gilberto Primel, Fabio Andrei Duarte e Bruno Meira Soares será publicado na revista Talanta. 📚 Este artigo é fruto do trabalho de mestrado da Maiara sob orientação do Prof. Bruno Meira, no Programa de Pós Graduação em Química Tecnológica e Ambiental (PPGQTA) da FURG. 📚 Para conferir mais, acesse o link abaixo e boa leitura! https://www-sciencedirect.ez40.periodicos.capes.gov.br/science/article/pii/S004896972200033X |
||
| 2022 | ||
|
Mais um trabalho acaba de ser publicado!!! Desta vez o trabalho “Does pH variation influence the toxicity of organic contaminants in estuarine sediments? Effects of Irgarol on nematode assemblages” de autoria de Mariana Aliceda Ferraz, Ana Carolina Kiyama, Ednei Gilberto Primel, Sergiane Caldas Barbosa, Ítalo Braga Castro, Rodrigo Brasil Choueri & Fabiane Gallucci oi publicado no periódico Science of the Total Environment. Este trabalho é fruto da parceria com o Prof. Ítalo Braga Castro (Universidade Federal de São Paulo). No trabalho, a equipe do LACOM atuou na determinação do biocida irgarol nas amostras de sedimento. 📚 Para conferir mais, acesse o link abaixo e boa leitura! https://www-sciencedirect.ez40.periodicos.capes.gov.br/science/article/pii/S004896972200033X
|
||
|
2021 |
||
|
Este trabalho é fruto do doutorado realizado pelo aluno Jean Lucas no Programa de Pós Graduação em Química Tecnológica e Ambiental, orientado pelo Prof. Ednei Gilberto Primel. Este trabalho propôs alternativas mais baratas, mais rápidas e principalmente, mais verdes do que os métodos oficiais para determinação de parabenos e alimentos. O grupo tem buscado como parte da sua missão, propor soluções que gerem menos resíduos, consumam menos produtos químicos e que exponham menos o analista, contribuindo assim com a Química Analítica Verde e o meio ambiente. Para conferir mais, clica aqui e boa leitura! |
||
|
2021 |
||
|
Desta vez o trabalho “DETERMINAÇÃO DE CONTAMINANTES EMERGENTES NO RIO LONTRA (SALTO DO LONTRA – PARANÁ)” de autoria de Pamela Koerich, Italo Kael Gilson, Marcos Geraldo Vieira, Sergiane Caldas Barbosa, Marina Raisa Vilela da Silva, Ednei Gilberto Primel, André Luiz Radunz, Liziara da Costa Cabrera foi publicado na Revista Biodiversidade. Este trabalho é fruto da parceria com a Prof. Liziara Cabrera (Universidade Federal da Fronteira Sul – UFFS, Campus Cerro Largo/RS) e resultado gerado de um trabalho de conclusão de curso, coordenado pela mesma. Os resultados deste tipo de trabalho trazem resultados importantes para a nossa sociedade, pois demonstram a presença de contaminantes presentes em esgotos domésticos em águas de superfície, as quais constituem compartimentos ambientais de muita importância, pois além de abrigar diferentes tipos de organismos e plantas, são muitas vezes usados como fonte de água para consumo humano após tratamento. Ressalta-se que o monitoramento desses compostos não é regulamentado pela legislação, existem poucos estudos no Brasil sobre a presença destes compostos no meio aquático. Durante o estudo, compostos presentes em filtro solares (avobenzona, benzofenona), estimulantes (cafeína), antiepilépticos (carbamazepina), anti-inflamatórios (diclofenaco sódico), anti helmínticos (mebendazol), conservantes (metilparabeno, propilparabeno) e antifúngicos (triclocarban e triclosan) foram detectados, confirmando a contaminação emergente nesse local. Para conferir mais, clica aqui e boa leitura! |
||
|
2021 |
||
|
Mais um trabalho fruto de colaboração internacional, do doutorado da aluna Karina Lotz Soares, orientada pelo Prof. Ednei Gilberto Primel, realizou o doutorado com período sanduíche no Instituto de Diagnostico Ambiental y Estudios del Agua (IDAEA) do Consejo Superior de Investigaciones Cientificas (CSIC), Espanha, através do projeto Ciências do Mar (2018). Lá, a aluna foi orientada pela Prof. Sílvia Díaz Cruz. Para conferir mais, clica aqui e boa leitura! |
||
|
||
|
2020 |
||
|
O artigo “Monitoramento de Fármacos e Produtos de Cuidado Pessoal (PPCPs) em Mananciais da Região Sudoeste do Paraná” acaba de ser publicado na revista Exatas On-Line”. Este trabalho é resultado da colaboração e interação que o LACOM mantém com ex integrantes do grupo. A Prof. Dra. Liziara da Costa Cabrera atuou por muitos anos no LACOM e hoje é docente e pesquisadora na Universidade Federal da Fronteira Sul (UFFS), Campus Realeza, Paraná. Para conferir mais, clica aqui e boa leitura! |
||
|
2020 |
||
|
Desta vez o trabalho “Validation of QuEChERS and GC-MS for pesticides determination in rice samples” de autoria de Sergiane Caldas Barbosa, Maristela Barnes Cerqueira, Ednei Gilberto Primel, Eliana Badiale Furlong e Larine Kupski foi publicado na Revista Mundi Engenharia, Tecnologia e Gestão. Este trabalho é fruto da parceria com a Prof. Larine Kupski (Universidade Estadual de Maringá, UEM) e resultado gerado do projeto Universal coordenado pela mesma. Além disso, esse trabalho tem colaboração com o Laboratório de Micotoxinas e Ciência de Alimentos coordenado pela Prof. Eliana Badiale Furlong. Para conferir mais, clica aqui e boa leitura! |
Limite de detecção
Vamos falar um pouco sobre o Limite de Detecção.
Quando são realizadas medidas em amostras com baixos níveis do analito ou de uma propriedade, como, por exemplo, análise de traços, é importante saber qual o menor valor de concentração do analito ou da propriedade que pode ser detectado pelo método.
Essa menor concentração do analito que pode ser detectado é justamente o limite de detecção.

Ele é determinado pela análise de amostras com concentrações conhecidas de analito ou por valores de propriedades conhecidos e pela definição de um nível mínimo em que o analito/propriedade pode ser detectado com confiança.
Existem diversas maneiras de calcular esse valor.





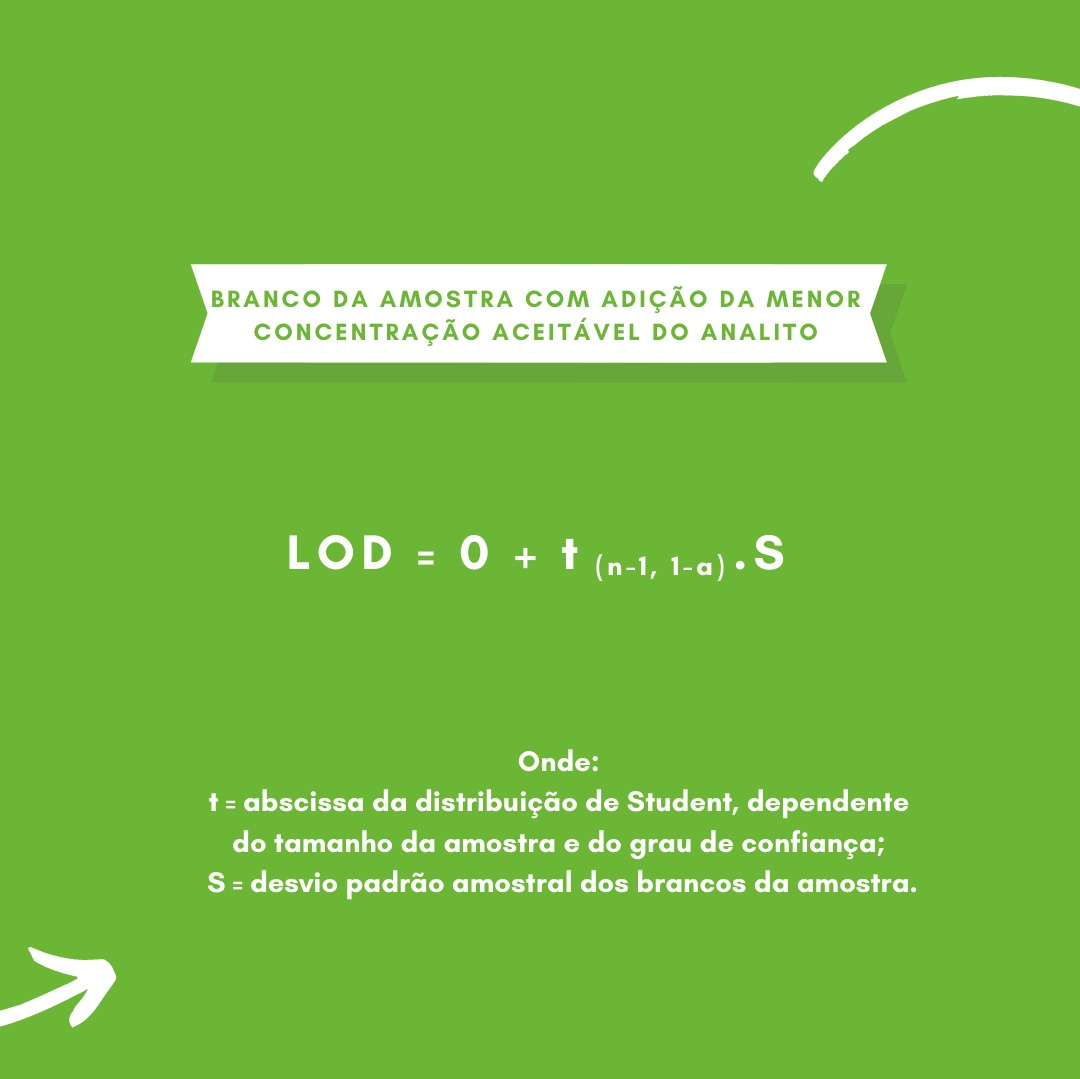

INMETRO. Orientações sobre validação de métodos analíticos (DOQ-CGCRE-008). Abril 2020. Disponível em: https://www.gov.br/inmetro/pt-br
LINEARIDADE
Vamos falar dos parâmetros de Linearidade, Faixa de Trabalho, Faixa Linear de trabalho e Sensibilidade, que, como vocês podem ver, estão muito conectados entre si.





Na última figura, vocês podem observar um exemplo de curva analítica com a identificação destes parâmetros.
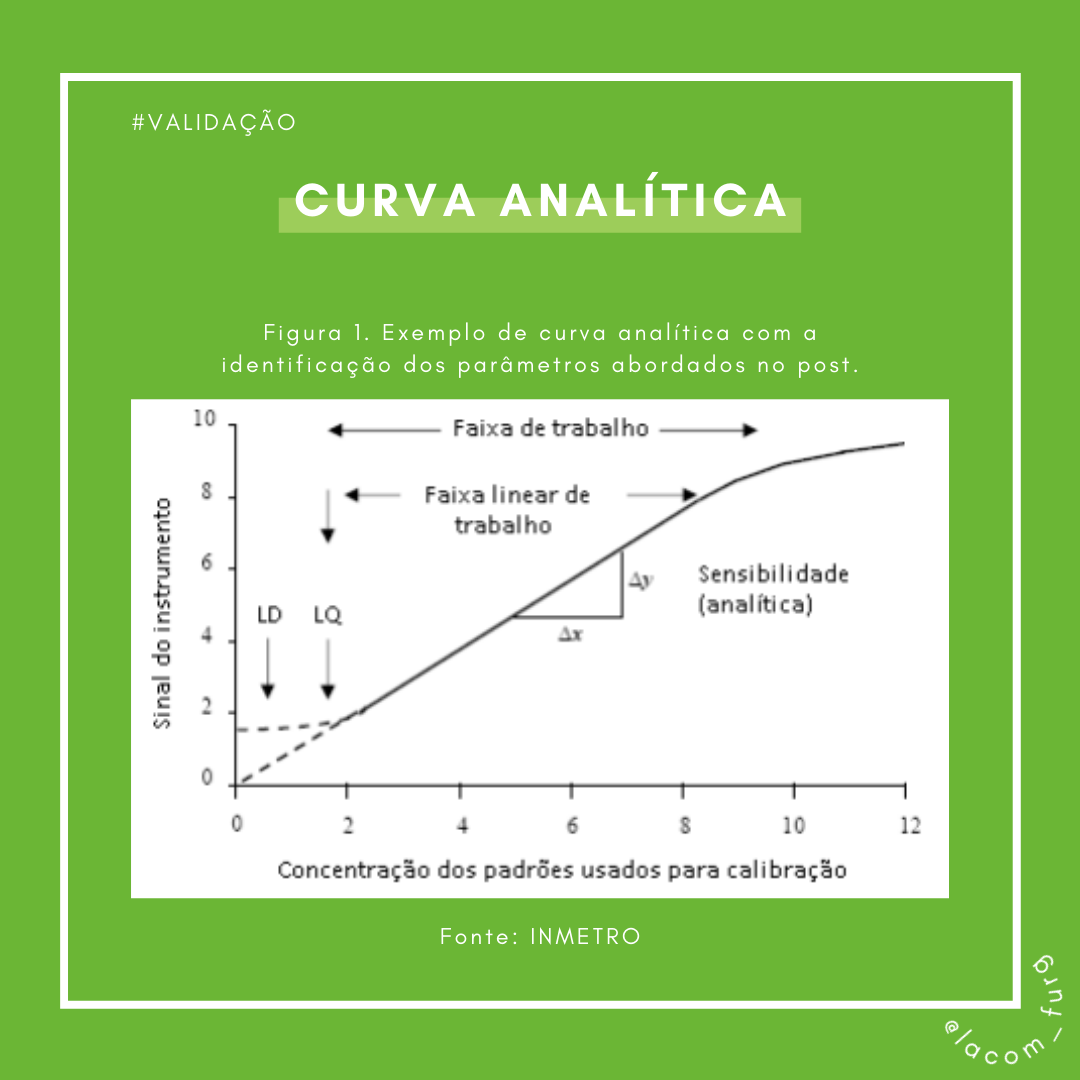
É importante lembrar alguns pontos:
A faixa de trabalho deve cobrir a faixa de aplicação para a qual o ensaio vai ser usado;
A concentração mais esperada da amostra deve, sempre que possível, se situar no centro da faixa de trabalho;
No limite inferior da faixa de concentração, o fator limitante é o valor do limite de quantificação, LOQ (futuro post);
No limite superior, os fatores limitantes dependem do sistema de resposta do equipamento de medição.
Para entender melhor como obter cada um destes parâmetros, sugerimos a leitura do documento “Orientação sobre validação de métodos analíticos” (DOQ-CGCRE-008) do INMETRO, que é a nossa referência para este post.
Restou alguma dúvida? Estamos aqui pra esclarecê-la.
SELETIVIDADE
O primeiro parâmetro da validação que estamos trazendo para vocês é a Seletividade!!
A seletividade avalia o grau de interferência de espécies, que podem ser outro ingrediente ativo, excipientes, impurezas e produtos de degradação, além também de outros compostos de propriedades similares que possam estar presentes.

Ela deve ser avaliada justamente porque esses interferentes podem aumentar ou reduzir o sinal do analito em estudo, além de que a magnitude do efeito também pode depender da concentração.
Se a seletividade não for assegurada, a linearidade, a tendência e a precisão estarão comprometidas, pois ela assegura que o pico da resposta é exclusivamente do composto que nos interessa. Não confunda um método específico com um método seletivo!!

O método seletivo pode produzir resposta para diversos analitos, no entanto, consegue diferenciar a resposta de cada um deles. Enquanto o método específico produz resposta apenas para um analito. Mas não se preocupe, há poucos métodos cromatográficos que respondem a apenas uma substância, então será mais frequente encontrar o termo “seletividade”.
Abaixo você encontra as duas formas mais utilizadas para se avaliar a seletividade.


Esperamos ter ajudado a sanar as tuas dúvidas sobre esse assunto. Caso contrário, contate-nos ou confere a referência para este post:
INMETRO. Orientações sobre validação de métodos analíticos (DOQ-CGCRE-008). Abril 2020. Disponível em: https://www.gov.br/inmetro/pt-br
VALIDAÇÃO
A validação é um dos procedimentos que mais realizamos no LACOM. Isso porque nós desenvolvemos métodos para identificação e quantificação de compostos, e para que esses novos métodos sejam considerados confiáveis e interpretáveis, é imprescindível que a validação seja realizada.
A validação tem o objetivo de confirmar que os métodos desenvolvidos são apropriados para o uso pretendido, através de estudos experimentais, a fim de garantir que o método atende às exigências das aplicações analíticas, assegurando a confiabilidade dos resultados.

Sendo assim, a validação engloba diversos parâmetros que devem ser avaliados conforme o ensaio necessite. Os parâmetros que são normalmente encontrados para validação de métodos de separação são: seletividade, linearidade/faixa de trabalho/sensibilidade, precisão, tendência/recuperação, limite de detecção, limite de quantificação e robustez.
No entanto, como comentado, aqueles que devem ser avaliados dependem do tipo de ensaio. Na figura abaixo, você pode conferir um quadro com os parâmetros que cada ensaio necessita.
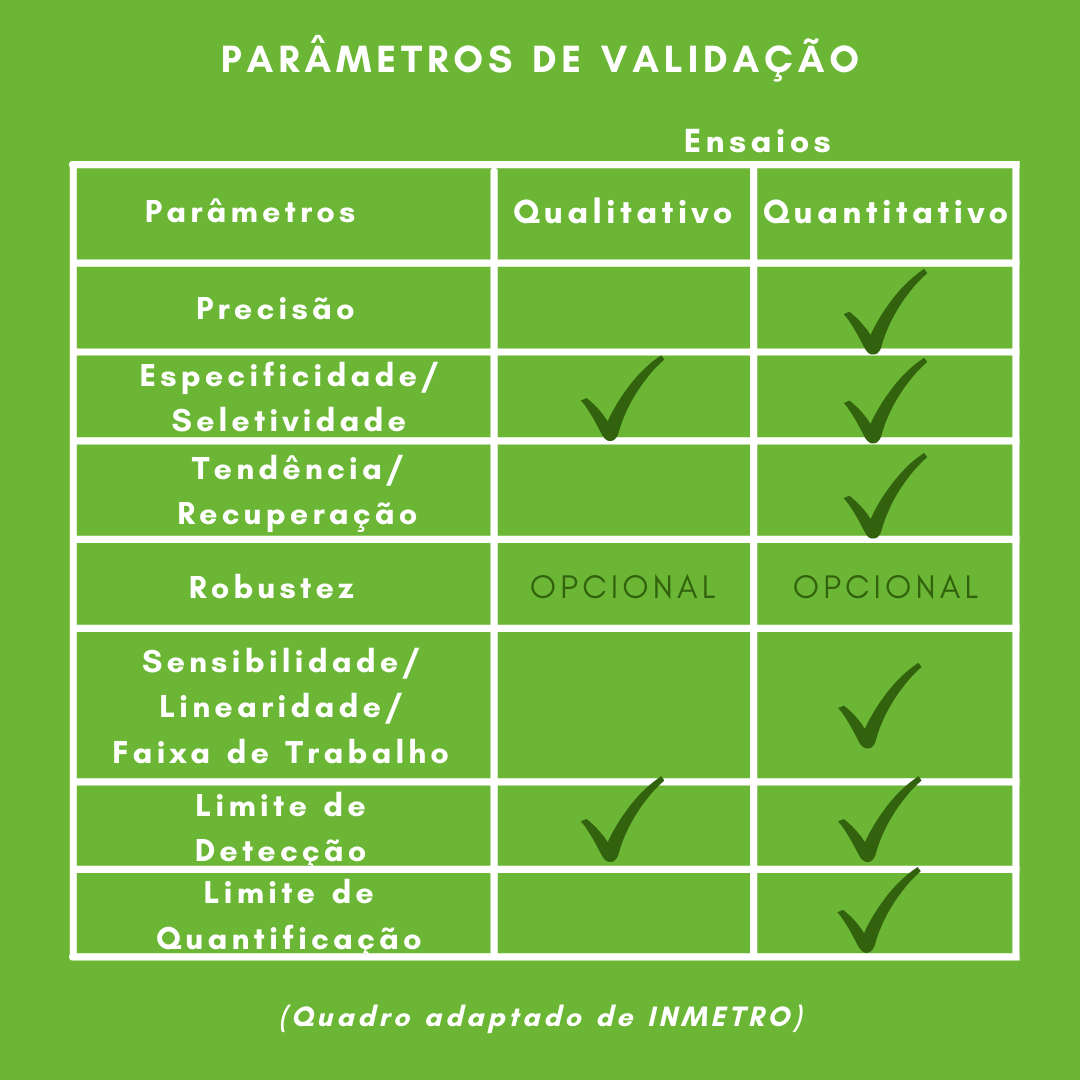
Esse quadro foi adaptado do INMETRO, que é, juntamente com a ANVISA, um órgão que disponibiliza guias para o procedimento de validação de métodos analíticos.
E aí, ficou claro? Esperamos que sim! Em caso de dúvida, entre em contato conosco ou acesse os sites dos órgãos citados.
INMETRO. Orientações sobre validação de métodos analíticos (DOQ-CGCRE-008). Abril 2020. Disponível em: https://www.gov.br/inmetro/pt-br
PARABENOS
Os Parabenos (PBs) são uma classe de PPCPs. produzidos através de uma reação de esterificação do ácido p-hidroxibenzoico, utilizando um álcool na presença de catalisador, como o ácido sulfúrico concentrado ou ácido p-toluenossulfônico.
Alguns exemplos de estruturas moleculares dos parabenos são mostradas na figura abaixo, onde a diferença entre eles se dá apenas na substituição da cadeia lateral.

Os parabenos são conhecidos por sua ação antimicrobiana e, portanto, são amplamente utilizados como conservantes em produtos cosméticos, fármacos, bebidas e diferentes tipos de alimentos.
A grande popularidade do uso de parabenos como conservantes se dá, principalmente, devido à muitas de suas propriedades intrínsecas, como por exemplo: amplo espectro de atividade antimicrobiana, estabilidade química, boa solubilidade e facilidade de produção.
Além disso, possuem a característica de não modificar o gosto, odor, consistência e coloração dos produtos em que são utilizados, além de serem econômicos e classificados como substâncias “geralmente consideradas seguras”, aprovadas para uso em alimentos pelo USA FDA.
Além de serem produzidos comercialmente, os parabenos podem estar presentes naturalmente nas plantas como antimicrobianos, além de serem produzidos por fermentação natural das plantas.
Agora, vamos abordar a importância de analisar os PBs.
Os seres humanos são expostos a esses compostos pelas vias dérmica (cosméticos), oral (alimentos/medicamentos) e por inalação.
Os PBs são absorvidos no intestino, metabolizados no fígado e excretados pela urina na forma livre ou na forma de dois biomarcadores: ácido p-hidroxibenzóico e ácido p-hidroxipurúrico.
Os PBs são os compostos mais comuns do grupo de produtos químicos desreguladores endócrinos, que têm habilidade de alterar o controle das funções fisiológicas do corpo (metabolismo, sono, humor, crescimento, etc.).
Embora os parabenos possam não ser a causa direta do câncer de mama e da endometriose, eles aumentam o risco carcinogênico para mulheres expostas. Além disso:
- Podem aumentar a proliferação de células de câncer de mama in-vitro;
- Induzir alterações uterinas relacionadas ao estrogênio;
- Causar alteração nos parâmetros reprodutivos de ratos machos;
- Entre outros.
Esses efeitos são diretamente relacionados ao comprimento da cadeia alquílica. Com o aumento da cadeia, há uma maior inibição do crescimento microbiano, já que também aumenta o valor do log Kow. Maiores valores de log Kow resultam em menor solubilidade em água, isso torna os parabenos compostos de caráter lipofílico e com potencial de bioacumulação.
Como a ingestão de alimentos é considerada uma fonte diária cumulativa de parabenos, regulamentos foram estabelecidos para garantir a segurança dos consumidores.
A esse respeito, o JECFA/OMS mostrou que uma ingestão diária aceitável (ADI, do inglês acceptable daily intake) de Metil e Etilparabeno considerada segura é de 10 mg/kg corporal/dia.

Em 2006, o Propilparabeno foi retirado do grupo de ADI pela FAO/WHO, devido aos efeitos adversos causados em estudos com ratos e, consequentemente, em 2008, foi proibido para utilização em alimentos pela ANVISA.
Assim, a determinação de parabenos, principalmente em alimentos, é essencial para garantir a boa saúde dos consumidores.
BELTIFA, A. et al. 2019.
BŁEDZKA, D. et al. Parabens. From environmental studies to human health. Environment International, 67, p. 27-42, 2014.
JO, A. et al. Influence of vegetarian dietary intervention on urinary paraben concentrations: A pilot study with 'temple stay' participants. Toxics, 8, n. 1, 2020.
LIAO, X. et al. A novel way to prepare n-butylparaben under microwave irradiation. Tetrahedron Letters, 43, n. 1, p. 45-48, 2002.
MAHER, H. M. et al. Quantitative screening of parabens in Ready-to-eat foodstuffs available in the Saudi market using high performance liquid chromatography with photodiode array detection. Arabian Journal of Chemistry, 13, n. 1, p. 2897-2911, 2020.
VILLAVERDE-DE-SÁA, E. et al. 2016.
ANALITOS
No LACOM, a maioria dos trabalhos envolve a análise de compostos químicos em amostras de alimentos ou ambientais. Esses compostos geralmente são Agrotóxicos ou Produtos Farmacêuticos e de Cuidado Pessoal (PPCPs, do inglês Pharmaceuticals and Personal Care Products), que incluem uma classe que também é muito analisada separadamente, os Parabenos.
AGROTÓXICOS
Vamos falar sobre os agrotóxicos.
Pela legislação brasileira, os agrotóxicos são definidos como “produtos e agentes de processos físicos, químicos ou biológicos, destinados ao uso nos setores de produção, no armazenamento e beneficiamento de produtos agrícolas, nas pastagens, na proteção de florestas nativas ou plantadas, e de outros ecossistemas e de ambientes urbanos, hídricos e industriais, cuja finalidade seja alterar a composição da flora ou da fauna, a fim de preservá-las da ação danosa de seres vivos considerados nocivos, bem como as substâncias e produtos empregados como desfolhantes, dessecantes, estimuladores e inibidores de crescimento”.
Os agrotóxicos abrangem muitas moléculas químicas, com diferentes modos de ação e toxicidade podendo ser classificados de acordo com a formulação, emprego, modo de ação e estrutura química.
Quanto à toxicidade os agrotóxicos são divididos em 4 classes:
I- extremamente tóxico
II-altamente tóxico
III-mediamente tóxico
IV-pouco tóxico
A principal classificação é quanto ao seu emprego, sendo classificados em inseticidas, herbicidas, fungicidas, acaricidas, moluscicidas, raticidas, entre outros.
Os agrotóxicos orgânicos sintéticos foram introduzidos imediatamente após a segunda Guerra Mundial, sendo que vários deles já serviram de arma química nas guerras da Coréia e do Vietnã, como o Agente Laranja (mistura de 2,4-D e 2,4,5 T), desfolhante que dizimou milhares de soldados e civis.
A introdução de agrotóxicos organossintéticos no Brasil teve início em 1943, quando chegaram às primeiras amostras do inseticida DDT. A agricultura praticada em nosso país ainda tem uma forte dependência da utilização de agrotóxicos, garantindo patamares mais elevados de produtividade.
Atualmente, é difícil imaginar a possibilidade de suprir a demanda mundial de alimentos sem o uso de agrotóxicos, pois tais produtos melhoram a produtividade agrícola, garantindo elevada produção..
O grande desafio é o uso adequado e com respeito às boas práticas agrícolas para diminuir ou evitar os danos ao meio ambiente.
Embora os agrotóxicos sejam utilizados na produção de alimentos, eles devem ser cuidadosamente usados e monitorados, porque podem ser tóxicos.
Uma parcela considerável do total aplicado para fins agrícolas atinge rios, lagos, aquíferos e oceanos por meio do transporte por correntes atmosféricas, eliminação incorreta de restos de formulações, limpeza de acessórios e recipientes empregados na aplicação desses produtos e pelo carreamento do material aplicado no solo pela ação erosiva da chuva. Devido aos mecanismos de transporte característicos dos meios aquáticos, alguns desses compostos têm sido detectados até na região Antártica.
A utilização de agrotóxicos é a segunda maior causa de contaminação dos rios no Brasil, perdendo apenas para o esgoto doméstico, segundo dados do IBGE.
Uma vez presente no ambiente aquático, estes compostos podem trazer prejuízos à biota ali presente. O impacto dos agrotóxicos depende do tipo de substância que foi utilizada e também da estabilidade do ambiente atingido. Nos casos mais graves, os agrotóxicos podem desencadear a morte de várias espécies de plantas aquáticas e animais, influenciando toda a comunidade aquática. Os agrotóxicos na água não atingem apenas espécies que vivem nesse ambiente. O homem, por exemplo, pode sofrer com a contaminação por agrotóxicos quando ingere um peixe que vive em uma área contaminada. Algumas espécies não morrem por causa do contato com os agrotóxicos, mas acabam acumulando-os em seu corpo. Esse acúmulo faz com que o produto seja passado através da cadeia alimentar, prejudicando, assim, outras espécies. Além disso, muitos desses mananciais são empregados para captação de água para consumo humano, e uma vez não eliminados no tratamento das estações de tratamento de água, estes podem estar na água consumida pela população.
Os seres humanos não estão isentos desta contaminação e alguns agrotóxicos podem acumular-se no organismo em tecidos lipídicos, fígado, rins, cérebro e coração. Como um agravante, muitos dos alimentos que fazem parte da dieta humana podem sofrer enriquecimento em relação à concentração inicial de agrotóxicos, como o leite, peixes de água doce ou salgada, crustáceos e vegetais.
Diversos estudos associam a exposição aos agrotóxicos comuns a inúmeras doenças, de asma a câncer, com destaque de maior risco para alguns grupos como agricultores, pessoas com imunidade baixa, idosos e crianças.
Fica claro então a importância do uso correto dos agrotóxicos, o respeito às boas práticas agrícolas e a necessidade de estudos de verificação de ocorrência, para garantia da saúde pública e do meio ambiente.
CALDAS, S. S.; ARIAS, J. L. O. ; ROMBALDI, C. ; MELLO, L. L. ; CERQUEIRA, M. B. ; MARTINS, A. F. ; PRIMEL, E. G. (2018) Occurrence of Pesticides and PPCPs in Surface and Drinking Water in Southern Brazil: Data on 4-Year Monitoring. JOURNAL OF THE BRAZILIAN CHEMICAL SOCIETY, 30, 71-80
Chiarello, M., Graeff, R.N., Minetto, L., Cemin, G., Schneider, V., & Moura, S. (2017). Determinação de agrotóxicos na água e sedimentos por HPLC-HRMS e sua relação com o uso e ocupação do solo. Química Nova, 40, 158-165.
PPCPs
MSPD
A Dispersão da Matriz em Fase Sólida (MSPD, do inglês Matrix Solid Phase Dispersion), foi introduzida por Barker e colaboradores em 1989, para a extração de resíduos de drogas em tecidos.
A MSPD está baseada na dispersão da amostra com auxílio de um suporte sólido que atua como abrasivo causando a ruptura da estrutura física da amostra.
O princípio básico da MSPD está baseado na pesagem da amostra, seguido da maceração desta com o suporte sólido. A dispersão é realizada por um tempo suficiente para que ocorra a completa homogeneização da amostra no suporte sólido e a ruptura da amostra em pequenas partículas.
Após a dispersão, a amostra e o suporte sólido formam uma fase única, que na técnica original é empacotada em uma coluna vazia, na qual é colocada uma frita (filtro de polietileno) antes e após o empacotamento. Após esta etapa, é realizada a eluição e o extrato está pronto para análise.
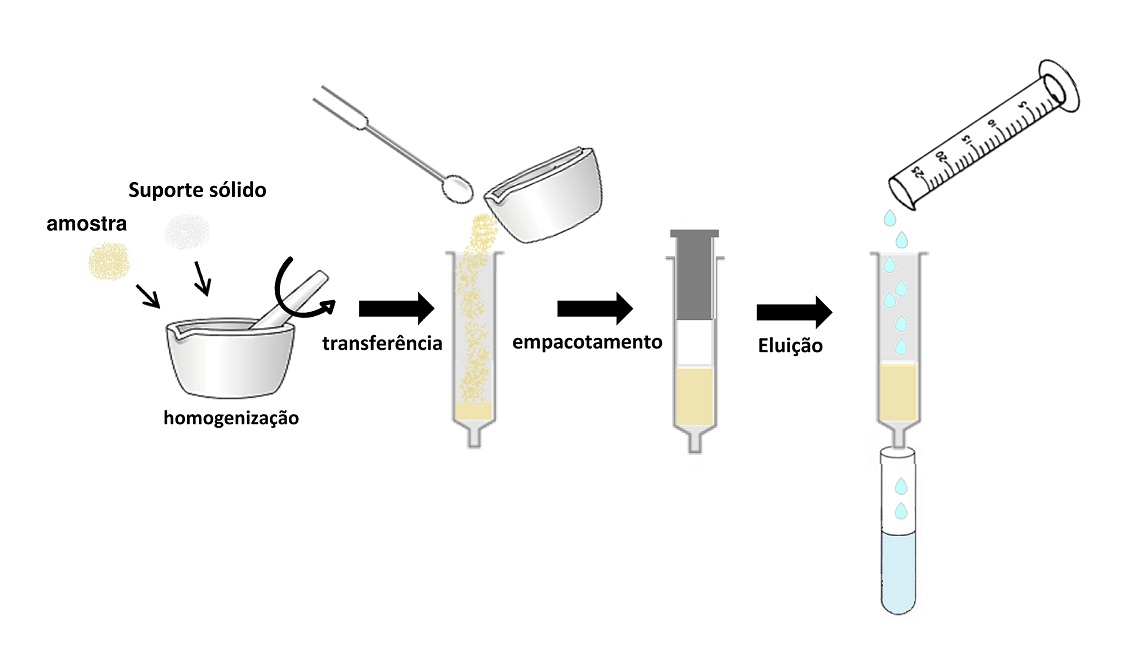
Já no LACOM, também utilizamos a VA-MSPD (Assistida por Vórtex, do inglês Vortex Assisted), que é uma modificação proposta pelo grupo e que utiliza as primeiras etapas semelhantes à MSPD original. A diferença está após a maceração, onde o macerado é transferido para o tubo em que será adicionado o solvente e então é levado ao vórtex e em seguida para a centrífuga. As fases são separadas e o sobrenadante (extrato) é retirado para análise.

O suporte sólido é um fator importante a ser otimizado na técnica da MSPD. Então aqui vão alguns exemplos de materiais clássicos utilizados: C18, C8, alumina, Florisil e sílica.
Além destes suportes tradicionalmente utilizados, materiais alternativos como polímeros molecularmente impressos (MIPs, do inglês Molecularly Imprinted Polymers), nanotubos de carbono de paredes múltiplas (MWCNTs, do inglês Multiwalled Carbon Nanotubes), terra diatomácea e areia também têm sido empregados na MSPD, bem como a ausência de suporte vem sendo avaliada.
No LACOM, a MSPD já foi utilizada para:
- Desenvolvimento de métodos para determinação simultânea de fármacos, filtros UV e biocidas em peixes (utilizando sílica como suporte sólido) e em sedimento (sem suporte sólido);
- Determinação de biocidas anti-incrustrantes em tecidos de pescado, com a utilização de concha de mexilhão como suporte sólido;
- Avaliar a presença de PPCPs em lodo de Estação de Tratamento de Esgoto, sem a utilização de suporte sólido;
- Desenvolvimento de método para determinação de espécies de mercúrio em peixes, utilizando sílica como suporte sólido;
- Desenvolvimento de método utilizando areia como suporte sólido na MSPD para extração multiclasses de agrotóxicos em frutas e hortaliças;
- Entre outros.
A grande vantagem da VA-MSPD está na possibilidade de realizar, em uma única etapa, a extração e a limpeza da amostra. Além disso, esta etapa geralmente é realizada à temperatura ambiente e pressão atmosférica, não necessitando de instrumentação para o controle destes parâmetros.
Além do que já foi exposto, é uma técnica que atende alguns dos princípios que nós do LACOM prezamos: os princípios da química analítica verde. Dentre eles, a MSPD é uma técnica que permite o uso de reagentes de fontes renováveis, pouca quantidade de amostra, gera pouco resíduo devido a empregar baixo volumes de solvente e baixa quantidade de amostra, demanda baixa quantidade de energia e proporciona maior segurança do analista, principalmente quando utilizada assistida por vortex.
Referência: FIGUEIREDO, E.C., BORGES, K. B., QUEIROZ, M.E.C., Preparo de amostras para análise de compostos orgânicos. 1 ed. Rio de Janeiro. 2015.
QuEChERS
Este post de preparo de amostra é sobre o método QuEChERS (do inglês Quick, Easy, Cheap, Effective, Rugged, Safe).
Este método foi desenvolvido no ano de 2003 por Anastassiades e colaboradores, com o objetivo de superar as limitações práticas dos métodos multirresíduos de extração de agrotóxicos em alimentos disponíveis na época.
O método tem como vantagens ser rápido, fácil, econômico, efetivo, robusto e seguro, sendo um procedimento dinâmico, capaz de ser realizado em qualquer laboratório. O método QuEChERS foi originalmente proposto para a extração de resíduos de agrotóxicos em frutas e vegetais, porém tem sido amplamente estudado para a determinação de diferentes compostos nas mais diversas matrizes.
O método é realizado em três etapas principais: A etapa de extração empregando como solvente, a acetonitrila, partição pela adição de sais e, por fim, uma etapa de limpeza do extrato empregando a extração em fase sólida dispersiva (dSPE).
Durante o desenvolvimento do método QuEChERS os autores buscaram descrever um método multirresíduo, que pudesse ser empregado tanto para a análise por LC quanto por GC. Desta forma, o uso de acetonitrila como solvente é adequado para ambas as técnicas cromatográficas, além de proporcionar a extração de diversos agrotóxicos com ampla faixa de polaridade e possibilitar menor extração de compostos lipofílicos presentes na matriz, como ceras, gorduras e pigmentos.
De maneira geral, o QuEChERS é um método barato e flexível. Seus principais parâmetros podem ser facilmente modificados e otimizados para melhorar a eficiência de extração e aumentar sua aplicação potencial em uma ampla gama de diferentes analitos e matrizes, sendo visto como uma alternativa confiável para o preparo de amostras.
Desde seu desenvolvimento o método QuEChERS tem passado por diferentes modificações para ser empregado na determinação de diferentes analitos em diferentes matrizes.
Com o objetivo de melhorar as recuperações para analitos sensíveis ao pH, foram propostas duas modificações do método QuEChERS.
A adição de uma etapa de tamponamento foi a primeira modificação proposta, Lehotay e colaboradores, em 2005 desenvolveram o método “QuEChERS-acetato”, no qual o efeito tamponante (pH 4,8) é promovido pela adição de acetato de sódio. Este método foi adotado em 2007 como método oficial da Association of Official Analytical Chemists (AOAC) para a determinação de resíduos de agrotóxicos em alimentos.
No ano de 2007, Anastassiades e colaboradores propuseram o método “QuEChERS-citrato”, este utiliza uma mistura de citrato de sódio di e sesquiidratados como responsáveis pelo efeito tamponante (pH 5,0 - 5,5). Em 2008, o European Committee for Standarisation, oficializou o método “QuEChERS citrato” como método de referência na União Europeia.
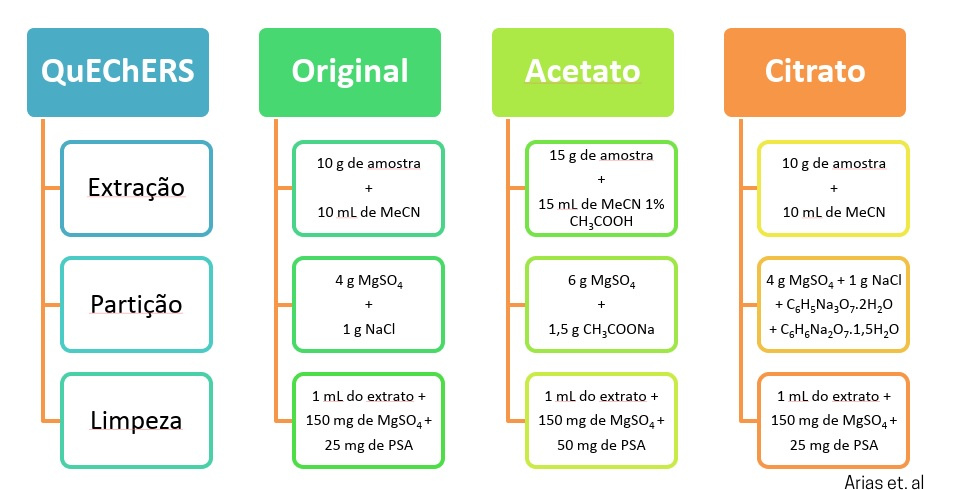
No Lacom, temos vários trabalhos que utilizaram o método QuEChERS:
-Determinação de parabenos em lodo de estação de tratamento de água.
-Avaliar a presença de agrotóxicos e hidroximetilfurfural em amostras de mel.
-Determinação de conservantes em diversos alimentos processados.
-Entre outros.
A maioria das modificações associadas ao método QuEChERS incluem a otimização das massas de amostra, quantidade e combinação de solventes e sais, sorventes para a etapa de limpeza, modos de agitação e miniaturização dos reagentes em geral, seguindo os princípios da Química Verde.
ANASTASSIADES, M. et al. Fast and easy multiresidue method employing acetonitrile extraction/partitioning and "dispersive solid-phase extraction" for the determination of pesticide residues in produce. Journal of AOAC International, v. 86, p. 412-431, 2003.
ARIAS, J.L.O. Fast and simple method of simultaneous preservative determination in different processed foods by QuEChERS and HPLC-UV: method development, survey and estimate of daily intake. FOOD CHEMISTRY, p. 112-119, 2019.
PRESTES, O. D. et al. QuEChERS - Um método moderno de preparo de amostra para determinação multirresíduo de pesticidas em alimentos por métodos cromatográficos acoplados à espectrometria de massas. Química Nova, v. 32, p. 1620-1634, 2009.
Preparo de amostras
Preparo de Amostras
Nos laboratórios de química analítica são realizados procedimentos para a identificação e quantificação de analitos (elementos, íons e moléculas) que constituem uma amostra. Para isso, são empregados métodos que são geralmente constituídos por duas técnicas, uma de preparo da amostra e outra para quantificação.
No LACOM nós desenvolvemos e validamos métodos para essa identificação e quantificação
Mas primeiramente, por que é preciso fazer um preparo da amostra?
O preparo da amostra é realizado com o objetivo de obter uma análise mais exata da amostra, uma vez que a matriz da amostra pode reduzir a habilidade de obter resultados exatos. Assim, com esse preparo podemos atingir melhores razões sinal-ruído, remover ou reduzir os interferentes e melhorar o desempenho da coluna analitica e do sistema cromatográfico.
Então, como no LACOM geralmente trabalha-se com matrizes complexas e os compostos presentes nelas, geralmente, estão em baixa concentração, o preparo de amostras é fundamental.
As técnicas possuem características diferentes, que serão abordadas nos próximos posts, podendo então eliminar possíveis interferentes e/ou concentrar os analitos.
Defesa de Memorial para Progressão a Classe Titular

O link para o evento é https://meet.google.com/rsd-twfi-prv e será transmitido pelo canal do youtube: Ednei Primel (https://www.youtube.com/channel/UC5DwNVkYcwpdv97_-bPIArQ/featured)
MS
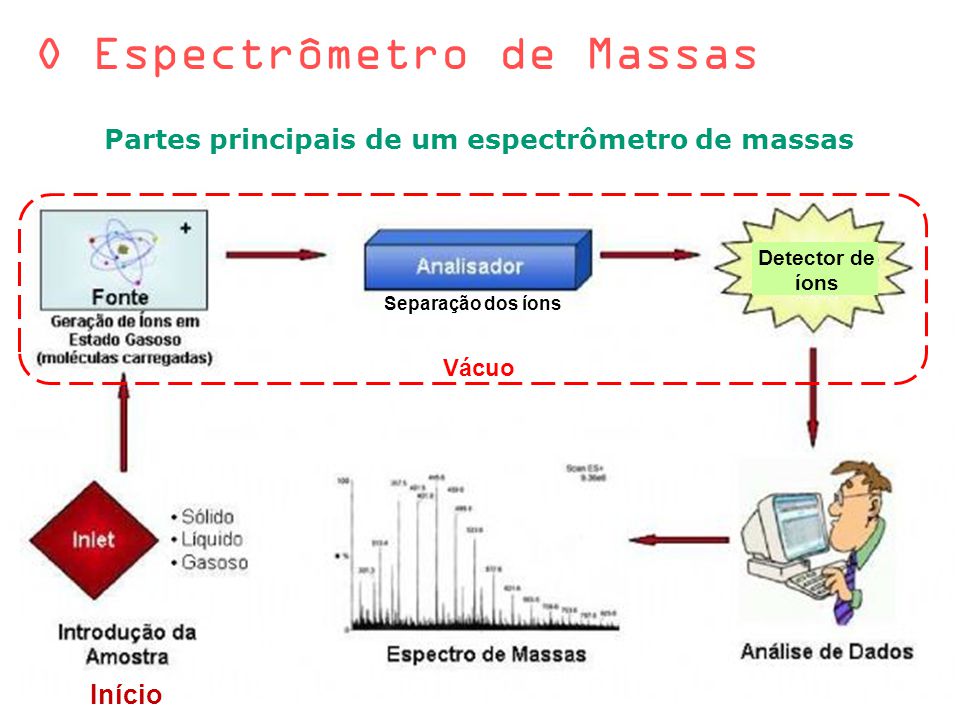
A espectrometria de massas (MS, do inglês mass spectrometry) é uma técnica analítica que utiliza da relação massa/carga (m/z) para caracterização, detecção e quantificação de analitos. Algumas aplicações: desenvolvimento de fármacos, identificação de moléculas em sangue e urina, monitoramento da qualidade do ar, água, entre outros. Os princípios da espectrometria de massas datam do fim dos anos 1890, quando J.J. Thomson determinou a razão m/z do elétron, e Wien estudou a deflexão magnética de raios anódicos determinando que os raios eram carregados positivamente. O primeiro espectrômetro de massa foi construído por A. J. Dempster, em 1918. Em sua forma mais simples o MS tem cinco componentes: a unidade de injeção da amostra, que traz a amostra do ambiente laboratorial (1 atm) para a pressão mais baixa do espectrômetro de massas; a fonte de íons, onde as amostras são transformadas em íons em fase gasosa. Os íons são então acelerados por um campo eletromagnético; o analisador de massas, que separa os íons da amostra baseado na sua razão massa/carga; o detector, que conta os íons; e o sistema de dados, que processa o sinal registrado, gerando o espectro de massas – um gráfico do número de íons detectados. No LACOM a fonte de ionização utilizada no HPLC é a ESI, em que a amostra é aplicada num capilar e na sua superfície é aplicado um potencial de alta voltagem. Pequenas gotículas da amostra serão carregadas e expulsas para câmara de ionização, onde o solvente irá evaporar da amostra, e em seguida a gotícula vai se dividir em outras menores, até formar a fase gasosa. Já no GC, utiliza-se a EI, que é composta por uma fenda para entrada da amostra, que vai receber um feixe de elétrons de alta energia formado através de um filamento que é aquecido até milhares de °C. Cátions sendo formados, serão repelidos por placas repelentes e ânodos. Essas placas tem potencial elétrico positivo, direcionando os cátions para outras placas, as placas aceleradoras e colimadoras. O analisador de massa será abordado com detalhes no próximo post.
Fonte: D. Pavia, Introdução à Espectroscopia, 2010

CD
No LACOM, o detector utilizado acoplado ao cromatógrafo de íons é o detector de condutividade (CD, do inglês conductivity detector). Esse tipo de detector é universal para as espécies carregadas e responde de uma forma previsível às alterações na concentração.
Além disso, esse detector é de simples operação, baixo custo de manutenção e, geralmente, operam por longos períodos sem necessitar de manutenção.
A condutividade é determinada como a resistência que um líquido produz entre dois eletrodos com uma área em uma distância.
O funcionamento deste detector está baseado na medida da capacidade da fase móvel em conduzir corrente quando posto em uma célula de fluxo entre dois eletrodos. A corrente dentro da célula vai depender do número e do tipo de íons presentes na fase móvel. As alterações na condutividade causadas pela presença dos analitos (íons) gera um sinal.
Uma limitação no uso de detectores de condutividade inicialmente foi a alta concentração de eletrólito necessária para a eluição da maioria dos íons dos analitos em um tempo razoável. Em consequência, a condutividade dos componentes da fase móvel tendem a se sobrepor à dos íons dos analitos, reduzindo, assim, a sensibilidade do detector.
Uma vez que eletrólitos aquosos são frequentemente usados como fase móvel em cromatografia de íons, o detector deve ser capaz de responder às mudanças relativamente pequenas na condutividade total do eluente causada pelos íons analisados. Então, em 1975, o problema criado pela alta condutância dos eluentes foi resolvido pela introdução de uma coluna supressora do eluente logo após a coluna trocadora de íons.
A coluna do supressor é recheada com uma segunda resina trocadora de íons que converte efetivamente os íons do solvente de eluição para espécies moleculares de ionização limitada sem afetar a condutividade dos íons dos analitos.
Pelo uso dessas técnicas de supressão, a condutividade de fundo de alguns eluentes pode ser drasticamente reduzida; no caso de ânions de ácido forte, é possível melhorar consideravelmente a sensibilidade.
Esse detector, acoplado ao cromatógrafo de íons, foi utilizado no LACOM para a determinação de halogênios em algas comestíveis, e também para o monitoramento de glifosato em amostras de água.
Fontes:
Skoog, D. A, West, D. M., Holler, F. J., Crouch, S. R. Fundamentos de Química Analítica, Editora Thomson, tradução da 8ª edição, 2006.
Metrohm. Práticas em Cromatografia de íons, tradução da 2ª edição, 2006.
DAD
DAD
No LACOM, utilizamos o HPLC acoplado ao Detector de Arranjo de Diodos (DAD), ou Detector de Arranjo de Fotodiodos (PDA), para a determinação de agrotóxicos em água subterrânea, conservantes em amostras de alimentos, entre outros.
O DAD faz parte do grupo de detectores de fótons e constitui a base dos instrumentos multicanais para absorção UV/visível.
Todos os detectores de fótons são baseados na interação da radiação com uma superfície reativa para produzir elétrons (fotoemissão) ou para promover elétrons para os estados energéticos nos quais podem conduzir eletricidade (fotocondução).
O DAD é composto por uma fonte de emissão de luz (lâmpada de deutério ou xenônio), que é colimada através de um sistema de lentes sobre a amostra. A luz total que passa através da célula contendo a amostra incide sobre uma grade holográfica. Essa grade difrata a radiação, separando seus diferentes comprimentos de onda, onde cada um deles incide sobre um diodo do arranjo. Este diodo, ao ser irradiado, produz uma corrente elétrica cuja magnitude está relacionada com a intensidade de emissão. Esta corrente é então transformada em absorbância nos diferentes comprimentos de onda através de um circuito, resultando no espectro de absorção da substância.
Os diodos são compostos por silício (Si) cristalino, que é um semicondutor, um material cuja condutividade elétrica é menor que a de um metal porém maior que a de um material isolante.
- COMO FUNCIONA A CONDUÇÃO?
O Si é um elemento do Grupo IV e dessa forma apresenta quatro elétrons de valência. Em um cristal de silício, cada um desses elétrons combina-se com os elétrons de outros quatro átomos de Si para formar quatro ligações covalentes.
À temperatura ambiente, ocorre uma agitação térmica suficiente nessa estrutura para ocasionalmente liberar um elétron de seu estado ligado, deixando-o livre para mover-se através do cristal.
A excitação térmica de um elétron deixa para trás uma região positivamente carregada denominada vacância (ou “buraco”), a qual, assim como o elétron, é móvel.
A movimentação da vacância ocorre por etapas, com um elétron ligado do átomo de silício vizinho saltando para a região deficiente de elétrons (a vacância) e assim criando outra vacância positiva. A condução em um semicondutor envolve o movimento de elétrons e de vacâncias em direções opostas.
- DIODOS
Os diodos são dispositivos semicondutores de junção pn* que respondem à luz incidente por meio da formação de pares elétron-vacâncias.
Um diodo de silício pode funcionar como um detector de radiação porque os fótons ultravioleta e visível são suficientemente energéticos para criar elétrons e vacâncias adicionais quando atingem a camada de depleção** da junção pn. O aumento da condutividade é medido facilmente e é diretamente proporcional à potência radiante.
Com um ou dois arranjos de diodos colocados ao longo da extensão do plano focal de um monocromador, todos os comprimentos de onda podem ser monitorados simultaneamente, tornando assim possível a espectroscopia de alta velocidade.
*Um semicondutor contendo elétrons não-ligados (cargas negativas) é chamado de semicondutor tipo “n” e um contendo um excesso de vacâncias (cargas positivas) é denominado tipo “p”. Em um semicondutor tipo n os elétrons são os portadores de carga majoritários; em um do tipo p, as vacâncias são os portadores majoritários; Junção pn: condutiva em uma direção, mas não em outra.
**Quando a maioria dos portadores de carga é drenada para fora da junção, origina-se a camada de depleção.
Fonte: Skoog, D. A, West, D. M., Holler, F. J., Crouch, S. R. Fundamentos de Química Analítica, Editora Thomson, tradução da 8ª edição, 2006.
SCOTT, R. P. W. Liquid Chromatography. Chrom-Ed Book Series-library4science, LLC, 2003.
FID
DETECTOR DE IONIZAÇÃO EM CHAMA - FID
O detector de ionização em chama (FID, do inglês Flame Ionization Detection), que é o detector mais empregado em aplicações da cromatografia gasosa em geral. Neste detector, o efluente da coluna é dirigido para uma pequena chama de ar/hidrogênio, onde a maioria dos compostos orgânicos produz íons quando “queimados”.
Na chama de ar/hidrogênio não existem íons, não conduzindo corrente elétrica. Quando um composto orgânico elui, e na sua queima são formados íons, a chama passa a conduzir corrente elétrica. Esse detector monitora a corrente produzida.
A ionização de compostos de carbono na chama é um processo ainda pouco compreendido, embora tenha sido observado que o número de íons produzidos é grosseiramente proporcional ao número de átomos de carbono “reduzidos” na chama.
Uma vez que o detector de ionização em chama responde ao número de átomos de carbono que entram no detector por unidade de tempo, ele é um dispositivo sensível à massa em vez da concentração. Em consequência, esse detector apresenta a vantagem de que a alteração da vazão da fase móvel exerce pouco efeito sobre a sua resposta, garantindo maior repetibilidade. Grupos funcionais como carbonila, álcool, halogênicos e amínicos produzem poucos ou nenhum íon na chama.
Essas propriedades tornam o detector de ionização em chama muito útil para a análise de amostras orgânicas, incluindo aquelas contaminadas com água e com óxidos de nitrogênio e enxofre. Uma desvantagem do detector de ionização em chama é que ele destrói a amostra durante a etapa de combustão.
No LACOM, esse detector foi utilizado para a determinação de glicerol, mono-, di- e triglicerídeos em biodiesel etílico de girassol, mamona e da mistura de sebo e soja; também foi utilizado para determinação de parabenos em amostras de camarão, biocidas em tecidos de peixes e atualmente vem sendo utilizado para determinar parabenos em amostras de alimentos.
Fonte: Skoog, D. A, West, D. M., Holler, F. J., Crouch, S. R. Fundamentos de Química Analítica, Editora Thomson, tradução da 8ª edição, 2006.
DETECTORES
DETECTORES
Vamos falar sobre os detectores que são utilizados acoplados aos cromatógrafos.
Um detector é um dispositivo que indica a existência de algum fenômeno físico.
Como exemplos de detectores utilizados no dia-a-dia estão o filme fotográfico (para indicar a presença de radiação eletromagnética ou radioativa), o ponteiro de uma balança (para indicar as diferenças de massas) e o nível de mercúrio em um termômetro (para indicar a temperatura).
O olho humano também é um detector, pois converte a radiação visível em sinais elétricos, que são transmitidos ao cérebro através de uma cadeia de neurônios presentes no nervo óptico e que produzem a visão.
Nos cromatógrafos, após a separação dos componentes da amostra, estes são “levados” ao detector, onde suas propriedades físicas e químicas são codificadas, processadas e convertidas em sinal elétrico.
Os detectores para cromatografia medem a variação da composição da fase móvel ao eluir da coluna cromatográfica, através de um sinal elétrico.
Esse sinal gerado pelo detector é interpretado através de um software instalado no computador, na forma de cromatogramas.
A quantificação é realizada através da área ou altura dos picos gerados nestes cromatogramas, que é proporcional à propriedade que se deseja observar, de acordo com o detector escolhido.
A escolha do detector dependerá da natureza da amostra e dos componentes a serem analisados, e consequentemente, do equipamento de separação.
Fonte: Skoog, D. A, West, D. M., Holler, F. J., Crouch, S. R. Fundamentos de Química Analítica, Editora Thomson, tradução da 8ª edição, 2006.
LACOM e a Semana Farroupilha

CROMATOGRAFIA DE ÍONS
A cromatografia de troca iônica ou cromatografia de íons (IC, do inglês Ion Chromatography) é uma subdivisão da HPLC (post anterior), e também é utilizada no LACOM.
Os conhecimentos sobre trocadores iônicos e suas aplicações foram expandidos entre 1935 e 1950, e foi em 1975 que o termo “cromatografia de íons” foi criado por Small, Stevens e Baumann.
Por definição, a IC é uma técnica sensível e seletiva aplicada na separação de íons, mesmo em baixas concentrações, utilizando-se uma coluna cromatográfica apropriada, seguida pela detecção. A detecção por condutividade (video ilustrativo no post) é a detecção padrão em IC mas também há a detecção por UV/VIS ou por amperometria. Basicamente, ela pode ser usada para determinar íons e moléculas polares.
O mais comum dos princípios de separação da IC é a troca iônica, que é baseada em uma reação química estequiométrica entre os íons de uma solução e uma substância sólida contendo os grupos funcionais, que podem fixar íons como resultado de forças eletrostáticas.
Teoricamente, íons com mesma carga podem ser completa e reversivelmente trocados entre as duas fases. Esse processo leva a uma condição de equilíbrio, sendo que o lado em que ocorre o equilíbrio depende da afinidade dos íons participantes em relação aos grupos funcionais da fase estacionária.
- APLICAÇÕES •
A área de aplicação mais importante da cromatografia de íons é a investigação de rotina dos sistemas aquosos (como a análise de água potável); ela também é usada a fim de resolver problemas de relevância ambiental e controle de ultratraços em processamento de reagentes ultrapuros requeridos principalmente na indústria de semicondutores.
Recentemente, essa técnica foi utilizada no LACOM para a determinação de halogênios em algas comestíveis, e também para o monitoramento de glifosato em amostras de água.
Fonte: Metrohm. Práticas em Cromatografia de íons, tradução da 2ª edição, 2006.

HPLC
A Cromatografia líquida de alta eficiência (do inglês, High Performance Liquid Chromatography) é uma técnica utilizada na separação dos vários componentes de uma mistura , com o objetivo de identificar, quantificar ou purificar esses componentes.
Essa técnica consiste no bombeamento de um solvente líquido (fase móvel) pressurizado contendo a amostra a ser analisada, que passa através de uma coluna preenchida com um material sorvente (fase estacionária). As substâncias com maior afinidade pelo solvente movem-se mais rapidamente; já as com menor afinidade movem-se mais lentamente. Ao eluir da coluna, os componentes passam por um detector que emite um sinal elétrico o qual é registrado, constituindo um cromatograma.
A cromatografia líquida foi definida quando o botânico russo Mikhail S. Tswett publicou o primeiro artigo no início de 1900 no qual ele descreveu a separação de pigmentos extraídos de plantas, utilizando solvente em uma coluna empacotada com partículas de carbonato de cálcio. Esse tipo de cromatografia obteve um avanço significativo a partir dos anos 70, e desde então vem apresentando avanços, dentre eles a utilização de colunas preenchidas por partículas de pequenos tamanhos, desenvolvimento e aperfeiçoamento de vários detectores por exemplo fluorescência, espectrofotômetros de massa acoplados ao HPLC, e dentre outros avanços que ocorreram desde a descoberta do equipamento.
•Aplicações•
A HPLC é utilizada em análises de compostos não voláteis ou termicamente instáveis onde a cromatografia a gás não pode ser utilizada. A HPLC pode ser utilizada em aplicações forenses, ambientais, farmacêuticas, alimentícias, entre outras. Como exemplo de trabalhos realizados no LACOM, podemos citar a quantificação de Fármacos e Produtos de Cuidado Pessoal e agrotóxicos em matrizes ambientais.
Fonte: Skoog. Fundamentos de Química Analítica, 2006.
Página 2 de 4