PARABENOS
Os Parabenos (PBs) são uma classe de PPCPs. produzidos através de uma reação de esterificação do ácido p-hidroxibenzoico, utilizando um álcool na presença de catalisador, como o ácido sulfúrico concentrado ou ácido p-toluenossulfônico.
Alguns exemplos de estruturas moleculares dos parabenos são mostradas na figura abaixo, onde a diferença entre eles se dá apenas na substituição da cadeia lateral.

Os parabenos são conhecidos por sua ação antimicrobiana e, portanto, são amplamente utilizados como conservantes em produtos cosméticos, fármacos, bebidas e diferentes tipos de alimentos.
A grande popularidade do uso de parabenos como conservantes se dá, principalmente, devido à muitas de suas propriedades intrínsecas, como por exemplo: amplo espectro de atividade antimicrobiana, estabilidade química, boa solubilidade e facilidade de produção.
Além disso, possuem a característica de não modificar o gosto, odor, consistência e coloração dos produtos em que são utilizados, além de serem econômicos e classificados como substâncias “geralmente consideradas seguras”, aprovadas para uso em alimentos pelo USA FDA.
Além de serem produzidos comercialmente, os parabenos podem estar presentes naturalmente nas plantas como antimicrobianos, além de serem produzidos por fermentação natural das plantas.
Agora, vamos abordar a importância de analisar os PBs.
Os seres humanos são expostos a esses compostos pelas vias dérmica (cosméticos), oral (alimentos/medicamentos) e por inalação.
Os PBs são absorvidos no intestino, metabolizados no fígado e excretados pela urina na forma livre ou na forma de dois biomarcadores: ácido p-hidroxibenzóico e ácido p-hidroxipurúrico.
Os PBs são os compostos mais comuns do grupo de produtos químicos desreguladores endócrinos, que têm habilidade de alterar o controle das funções fisiológicas do corpo (metabolismo, sono, humor, crescimento, etc.).
Embora os parabenos possam não ser a causa direta do câncer de mama e da endometriose, eles aumentam o risco carcinogênico para mulheres expostas. Além disso:
- Podem aumentar a proliferação de células de câncer de mama in-vitro;
- Induzir alterações uterinas relacionadas ao estrogênio;
- Causar alteração nos parâmetros reprodutivos de ratos machos;
- Entre outros.
Esses efeitos são diretamente relacionados ao comprimento da cadeia alquílica. Com o aumento da cadeia, há uma maior inibição do crescimento microbiano, já que também aumenta o valor do log Kow. Maiores valores de log Kow resultam em menor solubilidade em água, isso torna os parabenos compostos de caráter lipofílico e com potencial de bioacumulação.
Como a ingestão de alimentos é considerada uma fonte diária cumulativa de parabenos, regulamentos foram estabelecidos para garantir a segurança dos consumidores.
A esse respeito, o JECFA/OMS mostrou que uma ingestão diária aceitável (ADI, do inglês acceptable daily intake) de Metil e Etilparabeno considerada segura é de 10 mg/kg corporal/dia.

Em 2006, o Propilparabeno foi retirado do grupo de ADI pela FAO/WHO, devido aos efeitos adversos causados em estudos com ratos e, consequentemente, em 2008, foi proibido para utilização em alimentos pela ANVISA.
Assim, a determinação de parabenos, principalmente em alimentos, é essencial para garantir a boa saúde dos consumidores.
BELTIFA, A. et al. 2019.
BŁEDZKA, D. et al. Parabens. From environmental studies to human health. Environment International, 67, p. 27-42, 2014.
JO, A. et al. Influence of vegetarian dietary intervention on urinary paraben concentrations: A pilot study with 'temple stay' participants. Toxics, 8, n. 1, 2020.
LIAO, X. et al. A novel way to prepare n-butylparaben under microwave irradiation. Tetrahedron Letters, 43, n. 1, p. 45-48, 2002.
MAHER, H. M. et al. Quantitative screening of parabens in Ready-to-eat foodstuffs available in the Saudi market using high performance liquid chromatography with photodiode array detection. Arabian Journal of Chemistry, 13, n. 1, p. 2897-2911, 2020.
VILLAVERDE-DE-SÁA, E. et al. 2016.
ANALITOS
No LACOM, a maioria dos trabalhos envolve a análise de compostos químicos em amostras de alimentos ou ambientais. Esses compostos geralmente são Agrotóxicos ou Produtos Farmacêuticos e de Cuidado Pessoal (PPCPs, do inglês Pharmaceuticals and Personal Care Products), que incluem uma classe que também é muito analisada separadamente, os Parabenos.
AGROTÓXICOS
Vamos falar sobre os agrotóxicos.
Pela legislação brasileira, os agrotóxicos são definidos como “produtos e agentes de processos físicos, químicos ou biológicos, destinados ao uso nos setores de produção, no armazenamento e beneficiamento de produtos agrícolas, nas pastagens, na proteção de florestas nativas ou plantadas, e de outros ecossistemas e de ambientes urbanos, hídricos e industriais, cuja finalidade seja alterar a composição da flora ou da fauna, a fim de preservá-las da ação danosa de seres vivos considerados nocivos, bem como as substâncias e produtos empregados como desfolhantes, dessecantes, estimuladores e inibidores de crescimento”.
Os agrotóxicos abrangem muitas moléculas químicas, com diferentes modos de ação e toxicidade podendo ser classificados de acordo com a formulação, emprego, modo de ação e estrutura química.
Quanto à toxicidade os agrotóxicos são divididos em 4 classes:
I- extremamente tóxico
II-altamente tóxico
III-mediamente tóxico
IV-pouco tóxico
A principal classificação é quanto ao seu emprego, sendo classificados em inseticidas, herbicidas, fungicidas, acaricidas, moluscicidas, raticidas, entre outros.
Os agrotóxicos orgânicos sintéticos foram introduzidos imediatamente após a segunda Guerra Mundial, sendo que vários deles já serviram de arma química nas guerras da Coréia e do Vietnã, como o Agente Laranja (mistura de 2,4-D e 2,4,5 T), desfolhante que dizimou milhares de soldados e civis.
A introdução de agrotóxicos organossintéticos no Brasil teve início em 1943, quando chegaram às primeiras amostras do inseticida DDT. A agricultura praticada em nosso país ainda tem uma forte dependência da utilização de agrotóxicos, garantindo patamares mais elevados de produtividade.
Atualmente, é difícil imaginar a possibilidade de suprir a demanda mundial de alimentos sem o uso de agrotóxicos, pois tais produtos melhoram a produtividade agrícola, garantindo elevada produção..
O grande desafio é o uso adequado e com respeito às boas práticas agrícolas para diminuir ou evitar os danos ao meio ambiente.
Embora os agrotóxicos sejam utilizados na produção de alimentos, eles devem ser cuidadosamente usados e monitorados, porque podem ser tóxicos.
Uma parcela considerável do total aplicado para fins agrícolas atinge rios, lagos, aquíferos e oceanos por meio do transporte por correntes atmosféricas, eliminação incorreta de restos de formulações, limpeza de acessórios e recipientes empregados na aplicação desses produtos e pelo carreamento do material aplicado no solo pela ação erosiva da chuva. Devido aos mecanismos de transporte característicos dos meios aquáticos, alguns desses compostos têm sido detectados até na região Antártica.
A utilização de agrotóxicos é a segunda maior causa de contaminação dos rios no Brasil, perdendo apenas para o esgoto doméstico, segundo dados do IBGE.
Uma vez presente no ambiente aquático, estes compostos podem trazer prejuízos à biota ali presente. O impacto dos agrotóxicos depende do tipo de substância que foi utilizada e também da estabilidade do ambiente atingido. Nos casos mais graves, os agrotóxicos podem desencadear a morte de várias espécies de plantas aquáticas e animais, influenciando toda a comunidade aquática. Os agrotóxicos na água não atingem apenas espécies que vivem nesse ambiente. O homem, por exemplo, pode sofrer com a contaminação por agrotóxicos quando ingere um peixe que vive em uma área contaminada. Algumas espécies não morrem por causa do contato com os agrotóxicos, mas acabam acumulando-os em seu corpo. Esse acúmulo faz com que o produto seja passado através da cadeia alimentar, prejudicando, assim, outras espécies. Além disso, muitos desses mananciais são empregados para captação de água para consumo humano, e uma vez não eliminados no tratamento das estações de tratamento de água, estes podem estar na água consumida pela população.
Os seres humanos não estão isentos desta contaminação e alguns agrotóxicos podem acumular-se no organismo em tecidos lipídicos, fígado, rins, cérebro e coração. Como um agravante, muitos dos alimentos que fazem parte da dieta humana podem sofrer enriquecimento em relação à concentração inicial de agrotóxicos, como o leite, peixes de água doce ou salgada, crustáceos e vegetais.
Diversos estudos associam a exposição aos agrotóxicos comuns a inúmeras doenças, de asma a câncer, com destaque de maior risco para alguns grupos como agricultores, pessoas com imunidade baixa, idosos e crianças.
Fica claro então a importância do uso correto dos agrotóxicos, o respeito às boas práticas agrícolas e a necessidade de estudos de verificação de ocorrência, para garantia da saúde pública e do meio ambiente.
CALDAS, S. S.; ARIAS, J. L. O. ; ROMBALDI, C. ; MELLO, L. L. ; CERQUEIRA, M. B. ; MARTINS, A. F. ; PRIMEL, E. G. (2018) Occurrence of Pesticides and PPCPs in Surface and Drinking Water in Southern Brazil: Data on 4-Year Monitoring. JOURNAL OF THE BRAZILIAN CHEMICAL SOCIETY, 30, 71-80
Chiarello, M., Graeff, R.N., Minetto, L., Cemin, G., Schneider, V., & Moura, S. (2017). Determinação de agrotóxicos na água e sedimentos por HPLC-HRMS e sua relação com o uso e ocupação do solo. Química Nova, 40, 158-165.
PPCPs
MSPD
A Dispersão da Matriz em Fase Sólida (MSPD, do inglês Matrix Solid Phase Dispersion), foi introduzida por Barker e colaboradores em 1989, para a extração de resíduos de drogas em tecidos.
A MSPD está baseada na dispersão da amostra com auxílio de um suporte sólido que atua como abrasivo causando a ruptura da estrutura física da amostra.
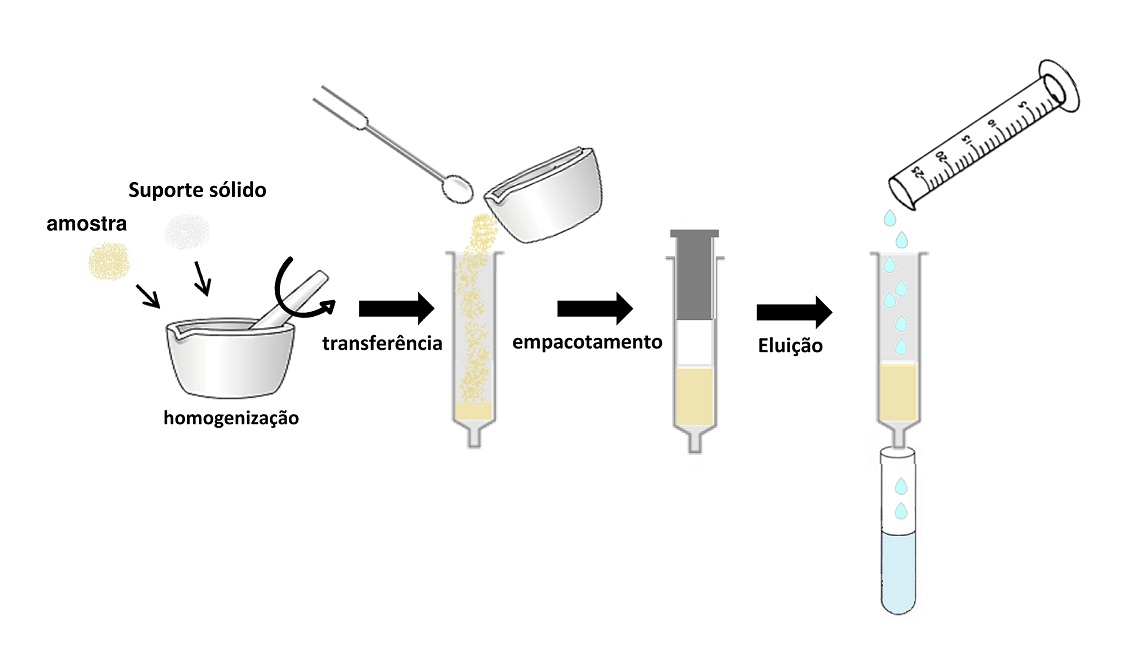
O princípio básico da MSPD está baseado na pesagem da amostra, seguido da maceração desta com o suporte sólido. A dispersão é realizada por um tempo suficiente para que ocorra a completa homogeneização da amostra no suporte sólido e a ruptura da amostra em pequenas partículas.
Após a dispersão, a amostra e o suporte sólido formam uma fase única, que na técnica original é empacotada em uma coluna vazia, na qual é colocada uma frita (filtro de polietileno) antes e após o empacotamento. Após esta etapa, é realizada a eluição e o extrato está pronto para análise.
Já no LACOM, também utilizamos a VA-MSPD (Assistida por Vórtex, do inglês Vortex Assisted), que é uma modificação proposta pelo grupo e que utiliza as primeiras etapas semelhantes à MSPD original. A diferença está após a maceração, onde o macerado é transferido para o tubo em que será adicionado o solvente e então é levado ao vórtex e em seguida para a centrífuga. As fases são separadas e o sobrenadante (extrato) é retirado para análise.

O suporte sólido é um fator importante a ser otimizado na técnica da MSPD. Então aqui vão alguns exemplos de materiais clássicos utilizados: C18, C8, alumina, Florisil e sílica.
Além destes suportes tradicionalmente utilizados, materiais alternativos como polímeros molecularmente impressos (MIPs, do inglês Molecularly Imprinted Polymers), nanotubos de carbono de paredes múltiplas (MWCNTs, do inglês Multiwalled Carbon Nanotubes), terra diatomácea e areia também têm sido empregados na MSPD, bem como a ausência de suporte vem sendo avaliada.
No LACOM, a MSPD já foi utilizada para:
- Desenvolvimento de métodos para determinação simultânea de fármacos, filtros UV e biocidas em peixes (utilizando sílica como suporte sólido) e em sedimento (sem suporte sólido);
- Determinação de biocidas anti-incrustrantes em tecidos de pescado, com a utilização de concha de mexilhão como suporte sólido;
- Avaliar a presença de PPCPs em lodo de Estação de Tratamento de Esgoto, sem a utilização de suporte sólido;
- Desenvolvimento de método para determinação de espécies de mercúrio em peixes, utilizando sílica como suporte sólido;
- Desenvolvimento de método utilizando areia como suporte sólido na MSPD para extração multiclasses de agrotóxicos em frutas e hortaliças;
- Entre outros.
A grande vantagem da VA-MSPD está na possibilidade de realizar, em uma única etapa, a extração e a limpeza da amostra. Além disso, esta etapa geralmente é realizada à temperatura ambiente e pressão atmosférica, não necessitando de instrumentação para o controle destes parâmetros.
Além do que já foi exposto, é uma técnica que atende alguns dos princípios que nós do LACOM prezamos: os princípios da química analítica verde. Dentre eles, a MSPD é uma técnica que permite o uso de reagentes de fontes renováveis, pouca quantidade de amostra, gera pouco resíduo devido a empregar baixo volumes de solvente e baixa quantidade de amostra, demanda baixa quantidade de energia e proporciona maior segurança do analista, principalmente quando utilizada assistida por vortex.
Referência: FIGUEIREDO, E.C., BORGES, K. B., QUEIROZ, M.E.C., Preparo de amostras para análise de compostos orgânicos. 1 ed. Rio de Janeiro. 2015.
Página 7 de 16