QuEChERS
Este post de preparo de amostra é sobre o método QuEChERS (do inglês Quick, Easy, Cheap, Effective, Rugged, Safe).
Este método foi desenvolvido no ano de 2003 por Anastassiades e colaboradores, com o objetivo de superar as limitações práticas dos métodos multirresíduos de extração de agrotóxicos em alimentos disponíveis na época.
O método tem como vantagens ser rápido, fácil, econômico, efetivo, robusto e seguro, sendo um procedimento dinâmico, capaz de ser realizado em qualquer laboratório. O método QuEChERS foi originalmente proposto para a extração de resíduos de agrotóxicos em frutas e vegetais, porém tem sido amplamente estudado para a determinação de diferentes compostos nas mais diversas matrizes.
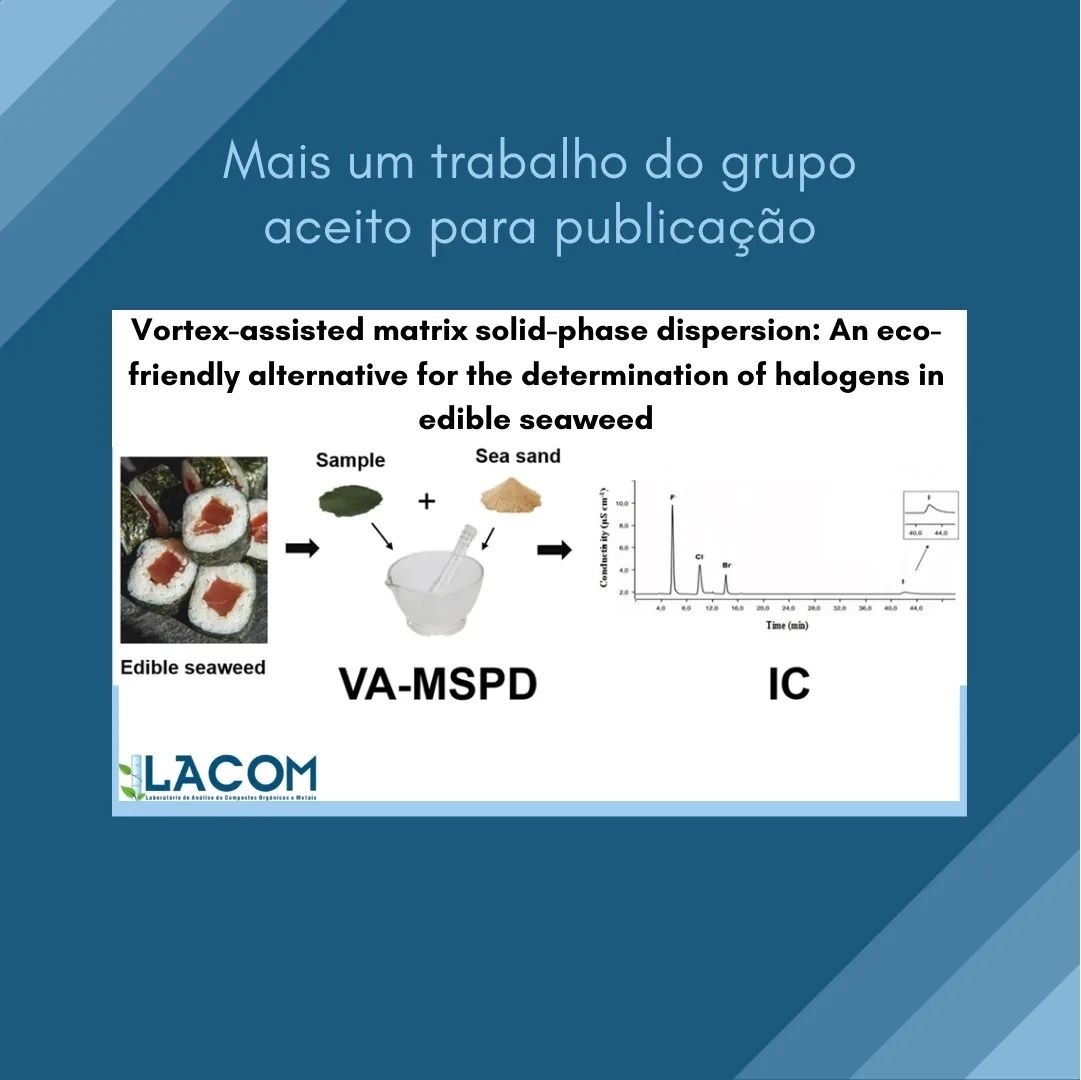
O método é realizado em três etapas principais: A etapa de extração empregando como solvente, a acetonitrila, partição pela adição de sais e, por fim, uma etapa de limpeza do extrato empregando a extração em fase sólida dispersiva (dSPE).
Durante o desenvolvimento do método QuEChERS os autores buscaram descrever um método multirresíduo, que pudesse ser empregado tanto para a análise por LC quanto por GC. Desta forma, o uso de acetonitrila como solvente é adequado para ambas as técnicas cromatográficas, além de proporcionar a extração de diversos agrotóxicos com ampla faixa de polaridade e possibilitar menor extração de compostos lipofílicos presentes na matriz, como ceras, gorduras e pigmentos.
De maneira geral, o QuEChERS é um método barato e flexível. Seus principais parâmetros podem ser facilmente modificados e otimizados para melhorar a eficiência de extração e aumentar sua aplicação potencial em uma ampla gama de diferentes analitos e matrizes, sendo visto como uma alternativa confiável para o preparo de amostras.
Desde seu desenvolvimento o método QuEChERS tem passado por diferentes modificações para ser empregado na determinação de diferentes analitos em diferentes matrizes.
Com o objetivo de melhorar as recuperações para analitos sensíveis ao pH, foram propostas duas modificações do método QuEChERS.
A adição de uma etapa de tamponamento foi a primeira modificação proposta, Lehotay e colaboradores, em 2005 desenvolveram o método “QuEChERS-acetato”, no qual o efeito tamponante (pH 4,8) é promovido pela adição de acetato de sódio. Este método foi adotado em 2007 como método oficial da Association of Official Analytical Chemists (AOAC) para a determinação de resíduos de agrotóxicos em alimentos.
No ano de 2007, Anastassiades e colaboradores propuseram o método “QuEChERS-citrato”, este utiliza uma mistura de citrato de sódio di e sesquiidratados como responsáveis pelo efeito tamponante (pH 5,0 - 5,5). Em 2008, o European Committee for Standarisation, oficializou o método “QuEChERS citrato” como método de referência na União Europeia.
No Lacom, temos vários trabalhos que utilizaram o método QuEChERS:
-Determinação de parabenos em lodo de estação de tratamento de água.
-Avaliar a presença de agrotóxicos e hidroximetilfurfural em amostras de mel.
-Determinação de conservantes em diversos alimentos processados.
-Entre outros.
A maioria das modificações associadas ao método QuEChERS incluem a otimização das massas de amostra, quantidade e combinação de solventes e sais, sorventes para a etapa de limpeza, modos de agitação e miniaturização dos reagentes em geral, seguindo os princípios da Química Verde.
ANASTASSIADES, M. et al. Fast and easy multiresidue method employing acetonitrile extraction/partitioning and "dispersive solid-phase extraction" for the determination of pesticide residues in produce. Journal of AOAC International, v. 86, p. 412-431, 2003.
ARIAS, J.L.O. Fast and simple method of simultaneous preservative determination in different processed foods by QuEChERS and HPLC-UV: method development, survey and estimate of daily intake. FOOD CHEMISTRY, p. 112-119, 2019.
PRESTES, O. D. et al. QuEChERS - Um método moderno de preparo de amostra para determinação multirresíduo de pesticidas em alimentos por métodos cromatográficos acoplados à espectrometria de massas. Química Nova, v. 32, p. 1620-1634, 2009.
Preparo de amostras
Preparo de Amostras
Nos laboratórios de química analítica são realizados procedimentos para a identificação e quantificação de analitos (elementos, íons e moléculas) que constituem uma amostra. Para isso, são empregados métodos que são geralmente constituídos por duas técnicas, uma de preparo da amostra e outra para quantificação.
No LACOM nós desenvolvemos e validamos métodos para essa identificação e quantificação
Mas primeiramente, por que é preciso fazer um preparo da amostra?
O preparo da amostra é realizado com o objetivo de obter uma análise mais exata da amostra, uma vez que a matriz da amostra pode reduzir a habilidade de obter resultados exatos. Assim, com esse preparo podemos atingir melhores razões sinal-ruído, remover ou reduzir os interferentes e melhorar o desempenho da coluna analitica e do sistema cromatográfico.
Então, como no LACOM geralmente trabalha-se com matrizes complexas e os compostos presentes nelas, geralmente, estão em baixa concentração, o preparo de amostras é fundamental.
As técnicas possuem características diferentes, que serão abordadas nos próximos posts, podendo então eliminar possíveis interferentes e/ou concentrar os analitos.
Defesa de Memorial para Progressão a Classe Titular

O link para o evento é https://meet.google.com/rsd-twfi-prv e será transmitido pelo canal do youtube: Ednei Primel (https://www.youtube.com/channel/UC5DwNVkYcwpdv97_-bPIArQ/featured)
MS
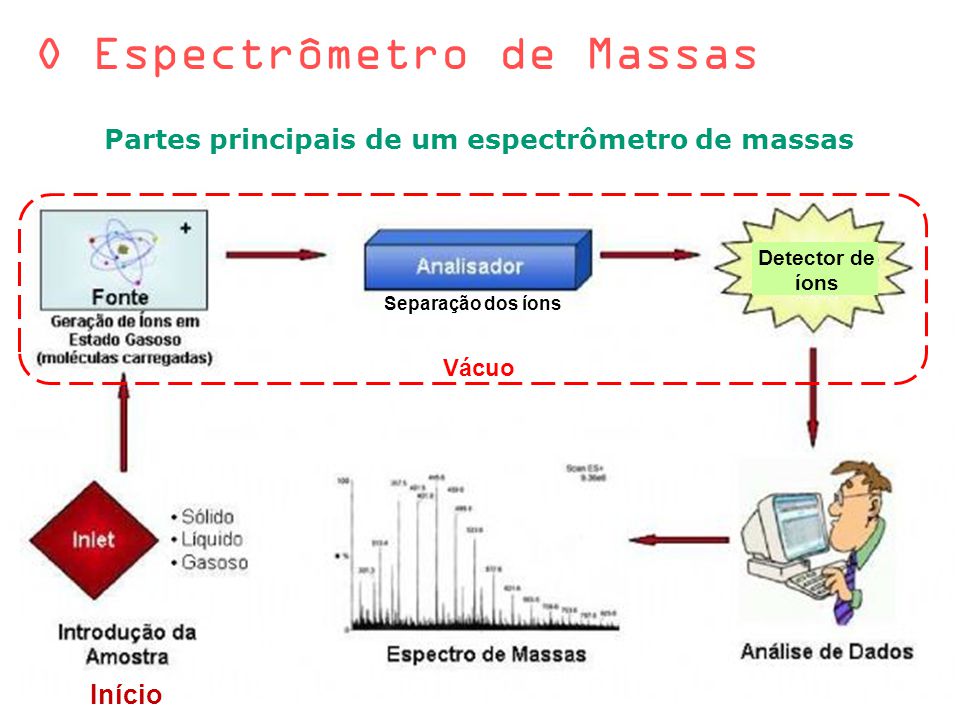
A espectrometria de massas (MS, do inglês mass spectrometry) é uma técnica analítica que utiliza da relação massa/carga (m/z) para caracterização, detecção e quantificação de analitos. Algumas aplicações: desenvolvimento de fármacos, identificação de moléculas em sangue e urina, monitoramento da qualidade do ar, água, entre outros. Os princípios da espectrometria de massas datam do fim dos anos 1890, quando J.J. Thomson determinou a razão m/z do elétron, e Wien estudou a deflexão magnética de raios anódicos determinando que os raios eram carregados positivamente. O primeiro espectrômetro de massa foi construído por A. J. Dempster, em 1918. Em sua forma mais simples o MS tem cinco componentes: a unidade de injeção da amostra, que traz a amostra do ambiente laboratorial (1 atm) para a pressão mais baixa do espectrômetro de massas; a fonte de íons, onde as amostras são transformadas em íons em fase gasosa. Os íons são então acelerados por um campo eletromagnético; o analisador de massas, que separa os íons da amostra baseado na sua razão massa/carga; o detector, que conta os íons; e o sistema de dados, que processa o sinal registrado, gerando o espectro de massas – um gráfico do número de íons detectados. No LACOM a fonte de ionização utilizada no HPLC é a ESI, em que a amostra é aplicada num capilar e na sua superfície é aplicado um potencial de alta voltagem. Pequenas gotículas da amostra serão carregadas e expulsas para câmara de ionização, onde o solvente irá evaporar da amostra, e em seguida a gotícula vai se dividir em outras menores, até formar a fase gasosa. Já no GC, utiliza-se a EI, que é composta por uma fenda para entrada da amostra, que vai receber um feixe de elétrons de alta energia formado através de um filamento que é aquecido até milhares de °C. Cátions sendo formados, serão repelidos por placas repelentes e ânodos. Essas placas tem potencial elétrico positivo, direcionando os cátions para outras placas, as placas aceleradoras e colimadoras. O analisador de massa será abordado com detalhes no próximo post.
Fonte: D. Pavia, Introdução à Espectroscopia, 2010

Página 8 de 16